Развитие цивилизации напрямую связано с развитием металлов. И не случайно в исторической классификации выделяют – Каменный век, Железный век, Бронзовый. Существует одна очень интересная легенда. Великие воины Трои были вооружены бронзовыми мечами, а их предводитель – булатным (стальным). Увы, секрет производства булатного оружия был потерян на долгие века. И лишь в середине прошлого столетия ученые вновь выяснили уникальную формулу.
Однако сегодня мы не будем говорить ни о химии, ни о металлургии. Мы поговорим о свойствах металла, о том, что они, подобно людям, запоминают, устают, стареют и даже поют! Если придерживаться исторических фактов – Бронзовый век начался примерно 6000 лет назад, Железный – 3000, и только 100 лет назад человечество освоило новые металлы, такие как - вольфрам, титан, ванадий.
Интересен и тот факт, что в биологических процессах жизнедеятельности живых организмов принимают участие металлы:
Целесообразно начать с классификации металлов. Критерий различия очень много. Можно выделить черные и цветные металлы, самородное состояние и сплавы и т.д. Однако, более полная характеристика металлов выглядит так:
Конечно, это далеко не полная классификация металлов.
В организме человека содержится такие металлы (при средней массе 70 кг):
Все свойства металла определяются его строением. Человек научился производить металлический сплав, обладающий памятью формы, т.е. изготовив из металла деталь, а потом ее видоизменить или деформировать, можно снова восстановить первичный вид. Металл помнит ту форму, которую ему придавали. Существуют сплавы, чья температура плавления гораздо ниже, чем у компонентов этого сплава. К примеру, температура плавления олова – 240 градусов Цельсия, а оловянный сплав плавится уже при 65 градусах. Существуют и так называемые псевдосплавы. Однако, прежде чем подробно о них говорить, лучше вспомнить теоритический материал, который накопили предшествующие поколения.
Металл имеет кристаллическую структуру. Это значит, что в его основе кристаллическая решетка, в углах которой находятся атомы, а вот между ними движется электронный газ. Т.е. каждый атом отдает по одному электрону, в т.н. общественный фонд. Электронный газ находится между узлами кристаллической решетки. Если, к примеру, взять кусок соли, кристаллическая структура четко видна. А если посмотреть на кусок металла, невозможно увидеть невооруженным глазом, что он состоит из кристаллов. Действительно, металлы состоят из поликристаллов (соединений нескольких кристаллов). Между ионами, которые находятся в узлах, и электронами, действует сила притяжения и отталкивания. Эти взаимодействия сил притяжения и отталкивания позволяют металлу сохранять свою форму. Обычно атомы находятся на самом низком энергетическом уровне, а взаимодействия сил притяжения и отталкивания между атомами создает определенное расстояние. Т.е. расстояние между атомами определяется силами притяжения и отталкивания.
Если необходимо увеличить расстояние между атомами, тогда силы притяжения возрастают. А если расстояние уменьшить, возрастут силы отталкивания. Наиболее выгодное энергетическое положение атомов в так называемой «ямке». Ее научное название – потенциальная яма.

График зависимости потенциальной энергии от расстояния
Энергия (Е) здесь отрицательная. Чем меньше значение «Е», тем выгоне энергетическое положение атома. Энергии соответствует определенное расстояние, которое определяется силами притяжения и отталкивания. В нижней части график симметричен. Если резко начать сжимать кристалл, то потенциальная энергия сразу возрастет, за счет того, что активизировались силы отталкивания. Если увеличить расстояние (значение Х возрастет), то начинают действовать силы притяжения, а показатель «Е» меняется. Если металл начать нагревать, график теряет симметричную форму. Этот подтверждает факт, что под действием высоких температур кристаллы меняют свою форму.
Нагревать металл можно при постоянном давлении, или изменчивом характере температуры и давления.

График нагрева металла при постоянном давлении
На графике видна своеобразная ступенька. Металл нагревается, температура «T» увеличивается, как и показатель времени «t». Наступает момент, когда время нагрева «t» продолжается, а «T» - температура остается неизменной. Это фазовый переход. В этот момент металл забирает энергию, но температура не растет. В этот момент металл меняет агрегатную форму – либо плавится (переходит из твердого в жидкий), либо испаряется (становится газообразным). Эта ступенька также помогает разобраться с принципом работы псевдосплавов.
Если нагревать металл с изменением давления и температур, то в итоге получим «диаграмму состояния».
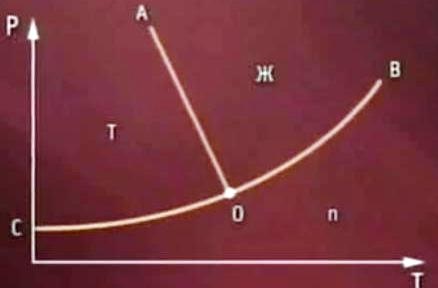
«Диаграмма состояния» для воды. (Она наиболее простая и понятная. Диаграммы для металлов гораздо сложнее).
На графике четко видны три состояния льда при нагреве – твердое, жидкое и газообразное. «О» – это тройная точка. В ней вода находится одновременно в трех агрегатных состояниях. Участок «О А» – фазовый переход. При этих параметрах вода переходит из твердого в жидкое состояние. «О В» – переход воды в газ. «С О» – вода из твердого состояния сразу же переходит в газообразное. Взяв два конкретных значения «Р» – давление и «Т» – температура, и отложив их на графике, сразу становится понятным агрегатное состояние воды. Если нагревать воду изобарически (давление остается константой), а температуру установить выше тройной точки, то график преобразуется в прямую линию. Если температуру установить ниже, чем тройная точка, то вода сразу перейдет из твердого в газообразное, минуя жидкое. Этот процесс называется возгонка. Простой пример классической возгонки – мороженное.
Теперь, зная теорию, перейдем к подробному разбору свойств и особенностей металлов.
Можно получить сплав, у которого температура плавления будет ниже, чем у компонентов, входящих в его состав, к примеру, сплав Вуда. Температура его плавления – 65 градусов Цельсия. В его составе (данные представлены в частях) Pb – 8; Sn – 4; Bi – 15; Cd – 3. Наиболее низкоплавкий компонент – олово Sn (температура плавления 230 градусов Цельсия). У остальных компонентов этот показатель гораздо выше.
А что произойдет, если из кристалла металла убрать свободные электроны, которые находятся между узлами кристаллической решетки? Как только исчезнут электроны, в узлах останутся ионы. Произойдет своеобразный взрыв, в результате которого кристалл распадется. Можно сделать вывод, что электронный газ, который находится внутри кристалла, стабилизирует весь кристалл.
Нужно заметить, что вся физика состоит из моделей. Они действительны до тех пор, пока мы можем объяснить их свойства. Если возникают трудности, тогда ищут ошибки. Если человек овладевает новой информацией, модель полностью переделывается с ее учетом. Кристаллическое строение металла это тоже модель.
Человечество использует металлы уже не первое тысячелетие своего существования. Этим веществам нашли применение в самых разных отраслях индустрии, в ювелирной промышленности, повседневном быту, и даже в медицине. В сегодняшние дни металл является незаменимым материалом для поддержания жизни цивилизации. Но как же человеку удалось его найти?
Некоторые металлы в природе пребывают в чистом виде. К таким относится золото, серебро, платина, поэтому неудивительно, что именно они были найдены первыми. Остальные же металлы, которые чаще всего можно найти в составе какой-нибудь руды, человек открыл многими веками позже. Интересную историю имеет медь, которая, хоть иногда и попадается в чистом виде, все же была получена из руды. А суть истории в том, что однажды наши предки обнаружили, что, кинув сплав меди в огонь, ее можно получить восстановленную в своем естественном виде. Это было поворотным моментом в развитии металлургии и, в частности, цивилизации.
Рассмотрим основные свойства металлов. Как уже говорилось, они могут быть как в чистом виде, так и находится в сплаве с другими металлами. К примеру, сплав меди с никелем образует мельхиор, с цинком - латунь, с оловом - бронзу. Бронзу люди умели получать еще несколько тысячелетий назад. Однако каким образом им это удавалось, современным металлургам достоверно не известно.
Важным свойством металлов является их электрическая и тепловая проводимость. В целях эксперимента соберем электрическую цепь, состоящую из источника тока и вольтметра. Замкнуть цепь мы по очереди попробуем проволоками из трех разных металлов: меди, железа и нихрома.
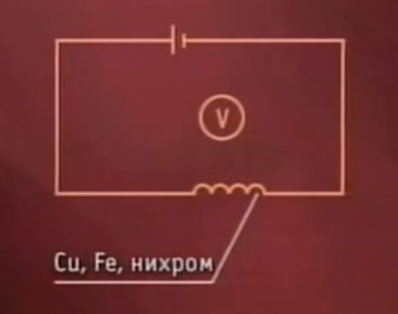
Электрическая цепь, которая состоит из источника тока и вольтметра.
Посмотрим, какую электропроводимость имеет каждый из них. Если замкнуть нашу цепь медью, то увидим, что стрелка вольтметра резко отклоняется. Используя в качестве проводника железо, можно заметить, что хоть стрелка на вольтметре и отклоняется, происходит это уже не с той силой. Это говорит о том, что железо имеет меньшую проводимость, нежели медь. И наконец, замкнем цепь нихромом. Стрелка вольтметра не сдвинулась, что говорит о нулевой проводимости нашего материала. Но чем обусловливается настолько разная электропроводимость металлов? Здесь мы обратимся к важнейшему закону электрики, который каждый наверняка помнит еще со школьных времен.
Закон Ома был выведен экспериментально примерно за 15 лет. Великий физик Георг Симон Ом имел при жизни репутацию чудака, так как был преподавателем, на которого ученики смотрели как на сумасшедшего, ввиду того, что после уроков тот занимался своими экспериментами и вообще заявлял, что его закон однажды станет главным законом физики. Однако теперь мы знаем, что ученый не зря потратил долгие годы исследований, за что заслуженно получил высокую научную степень и признание коллег. Но вернемся к делу.
Закон Ома гласит, что сила тока равна напряжению, поделенному на сопротивление. В сегодняшние дни это очевидный факт, но есть некоторые детали, на которые хотелось бы обратить внимание. Металл состоит из кристаллической решетки, в узлах которой находятся атомы, а между ними хаотично двигаются электроны. Как только на металл подается напряжение, электроны начинают двигаться направленно, в ином случае электрического тока быть не может. И раз появилась сила, способная заставить электроны двигаться в определенном направлении, то по закону Ньютона частицы должны двигаться с ускорением, и сила тока должна расти. Но этому факту противоречит закон Ома, согласно которому для повышения силы тока необходимо повысить напряжение. Поэтому, электроны металла хоть и двигаются, делают они это с постоянной скоростью. Видимо, есть еще какая-то сила, которая их тормозит. Но что бы это могло быть? Сложный вопрос. Назовем это дефектами, но это уже отдельная тема.
Еще одно интересное свойство металлов – тепловая проводимость. В этом явлении загадок не меньше, чем в электропроводимости. Вообще у кристалла своеобразное поведение. Если подвести к нему тепло, то появляется электрический ток, при этом электроны кристалла на тепло не реагируют! Но эта тема слишком сложна, поэтому не будем в нее углубляться в данной статье.
Как объяснить же химическое строение металлов? Забавно, что физики частенько посмеиваются над химиками, так как считают, что загадок в химических реакциях уже нет, потому что все химические реакции объясняются взаимодействием электронов. Физика считает, что она все уже объяснила и загадок больше нет. Но давайте все-таки рассмотрим свойства металлов.
Существует так званная зонная теория, которая говорит о том, что электроны расположены вокруг атома на различных энергетических уровнях, причем на одном таком уровне не может быть больше двух электронов. Так вот если нагреть металл, то электроны могут переходить из одного уровня на другой. Но переходить могут только с последнего уровня, так как более низкие уровни обычно уже заняты электронами. Именно поэтому при нагревании электроны не вносят свой вклад в теплоемкость.

Схема зонной теории
Рассмотрим строение металлов подробнее. Вспомним, что химическая активность элементов зависит от строения электронных оболочек. На таблице видим, что есть энергетические уровни (K, L, M, N), каждый уровень имеет подуровни (s, p, d). Каждый подуровень может принять в свою ячейку определенное количество электронов. Обратите внимание на неон «Ne», его электроны заняли все возможные уровни и ячейки. Больше нет частиц, которые могли бы занять следующие ячейки. Именно поэтому неон является инертным газом – его химическая активность предельно низкая. Другое дело калий «K», химическая активность которого более высокая ввиду меньшей заполненности энергетических уровней. Из этого всего мы можем сделать заключение, что активность элементов напрямую зависит от расположения электронов, и металлы не являются исключением.
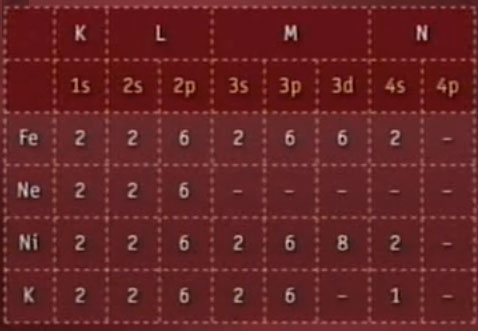
Таблица позволяющая доказать, что активность элементов (в том числе металлов) зависит от строения электронных оболочек, от взаимодействия электронов.
Вспомним очередное любопытное свойство металлов - коррозию. Она является проблемой как бытового, так и глобального уровня. Коррозия приводит к гибели металла. Что особенно интересно - коррозионная активность в атмосфере нашей планеты растет. Второй, не менее интересный факт – самая низкая подверженность металла коррозии в Антарктиде, а самая высокая - на экваторе и в близкой к океанам и морям местности. Приведем реальные цифры по скорости коррозии: в Антарктиде коррозия железа составляет 0,05 мкм (микрометра) в год, меди – 0,07 мкм в год. На экваторе коррозия железа равна 958 мкм в год, меди – 7,5 мкм в год. Вот такие интересные данные имеем по зависимости коррозии от нахождения металла на том или другом участке Земли.
Важным моментом в эксплуатации металлов является то, что их приходится использовать при температурах, которые выше их температуры плавления. То есть, допустим, что температура плавления металла равна 3 тыс. градусов Цельсия, а использовать его необходимо при температуре 4 тыс. градусов. Однако и эту проблему человечество смогло решить. Например, берется самый тугоплавкий элемент - вольфрам, и чтобы он не плавился при высокой температуре, его напыляют слоем меди. Конечно же, у меди температура плавления меньше. Однако пока медь будет испаряться под действием температуры, вольфрам останется нетронутым. Конечно, долго данный процесс продолжаться не может, но на практике (например, для космических целей) этого времени вполне достаточно, чтобы выполнить необходимые задачи.
Интересно, а как же создают металлы, запоминающие свою форму? Для понимания технологии будем пользоваться двумя металлургическими терминами – мартенситная фаза и аустенитная фаза. Возьмем проволоку никеля и нагреем ее до аустенитной фазы, после чего дадим ей остыть до мартенситной фазы. В результате чего проволока запомнит ту конструкцию, которую мы дадим ей во время тепловой обработки. А потом мы возьмем нашу конструкцию и сожмем. Казалось бы, вернуть ее прежнюю форму теперь невозможно. Однако достаточно просто нагреть ее, и металл вспомнит форму, которую мы ему придали. Конечно, мы очень упростили описание этого процесса. В реальности для его осуществления нужны сложные расчеты, тем не менее, такая технология работает, и даже в 70-е годы прошлого века ее хотели применять для выправления позвоночника. Вот такие интересные эксперименты проводились с металлами всего полвека назад.
С металлами связаны даже космические проблемы. Например, на звездах происходят разнообразные процессы превращения (например, водород превращается в углерод), и доказано, что, как только процесс превращения доходит до железа, т.е. начинается в процессе термоядерных реакциях проявляться железо, звезда погибает. Это явление - еще один яркий пример, как металлы способны влиять на окружающую нас среду.
В этой статье мы рассмотрели основные свойства металлов, знание которых помогает нам использовать эти вещества в самых разных сферах своей жизнедеятельности, а также углубляет наше понимание разных явлений, как на поверхности Земли, так и во всей вселенной.
Просто и выгодно, сдача металлолома по всей Украине! Находим по нашему КАТАЛОГУ нужную металлоломную компанию своего региона. Звоним, узнаем цену на лом, договариваемся об условиях вывоза-приема и вуаля, Вы получаете денежное вознаграждение и делаете большой плюс экономике и экологии.
Государственные стандарты Украины:
ГОСТ (ДСТУ) 4121–2002 "Металлы черные вторичные" и
ГОСТ 1639:2009 (ДСТУ 3211:2009) "Лом и отходы цветных металлов и сплавов".